La condizione di reversibilità o irreversibilità di una trasformazione, formulata dal secondo principio della termodinamica, può essere espressa in funzione della variazione dell'entalpia e dell'entropia del sistema tra due stati 1 e 2. A pressione costante, il calore scambiato dall'ambiente con il sistema alla temperatura T, indicato come ΔSamb., è uguale al ΔH del sistema cambiato di segno. Pertanto, il secondo principio può essere riscritto come:
Moltiplicando entrambi i membri per -T e cambiando il segno della disuguaglianza, si ottiene:
Ponendo:
si ha che ΔG rappresenta la variazione di una funzione di stato, chiamata energia libera di Gibbs (G), quando il sistema passa da uno stato iniziale 1 a uno stato finale 2 a temperatura T e a pressione costante.
L'introduzione della funzione di stato energia libera, definita dalla relazione:
consente di riscrivere il secondo principio in termini di grandezze termodinamiche che si riferiscono al solo sistema. La reversibilità (stato d'equilibrio) o irreversibilità (spontaneità) di una trasformazione sono espresse dalla condizione: ΔG ≤ 0.
- Per ΔG < 0, la trasformazione è spontanea.
- Per ΔG = 0, il sistema è all'equilibrio.
- Per ΔG > 0, la trasformazione non è spontanea.
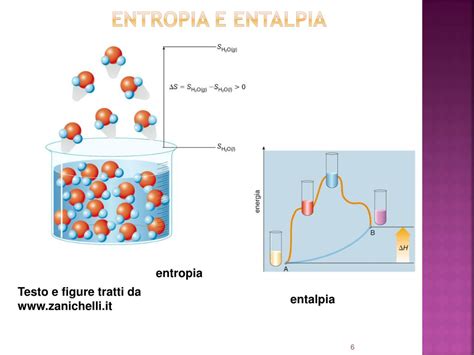
L'energia libera, espressa in funzione dell'entalpia e dell'entropia del sistema, tiene conto della tendenza dei sistemi a evolvere spontaneamente verso stati di minima energia e massima entropia (massimo disordine). Le trasformazioni spontanee sono favorite dal segno negativo del ΔH e dal segno positivo del termine TΔS. Nei casi in cui uno dei segni sia sfavorevole alla spontaneità, il segno di ΔG dipende dal peso relativo dei due termini. Quando entrambi i segni sono sfavorevoli, la trasformazione non è spontanea.
Energia Libera Molare Standard e Variazione di Energia Libera Standard
L'energia libera molare standard di una specie chimica è l'energia libera di formazione (ΔG°f) di una mole di composto nel suo stato standard a partire dagli elementi, anch'essi nel loro stato standard (ai quali, in queste condizioni, viene attribuita un'energia libera standard uguale a zero).
La variazione di energia libera standard (ΔG°) di una reazione è espressa dalla relazione:
Il ΔG° è una costante, per una determinata reazione, che dipende dalla natura chimica di reagenti e prodotti. Il suo valore numerico consente di valutare quantitativamente la spontaneità della reazione. In genere, per comodità, si riportano i dati alla temperatura di 298 K, ma la definizione di stato standard non dipende dalla temperatura.
È possibile calcolare l'energia libera standard di una reazione utilizzando l'energia libera standard di formazione delle specie chimiche che prendono parte alla reazione:
dove ciascun ΔG°f è moltiplicato per il coefficiente stechiometrico di reazione.
La reazione c(s) diamante → c(s) grafite ha un cambiamento negativo nell'energia libera di Gibbs e pertanto è spontanea a 25 °C e 1 atm. La reazione avviene troppo lentamente per essere osservata in quanto la sua energia di attivazione è molto elevata.
Relazione tra Energia Libera, Lavoro Utile e Condizioni di Reazione
Il ΔG è la misura del lavoro massimo ottenibile da un processo spontaneo, se questo fosse condotto in condizioni di reversibilità. In pratica, nelle trasformazioni reali il lavoro utilizzabile è sempre inferiore al ΔG della trasformazione, e tanto più si avvicina ad esso quanto più la trasformazione viene realizzata in condizioni che si avvicinano alla reversibilità.
Per una generica reazione:
la variazione di energia libera è data dalla seguente espressione (detta isoterma di reazione):
dove il rapporto sotto logaritmo ha la forma della costante d'equilibrio, ma i valori delle concentrazioni, espresse in moli/litro, [C], [D], [A], [B] si riferiscono a un determinato istante durante lo svolgersi della reazione.
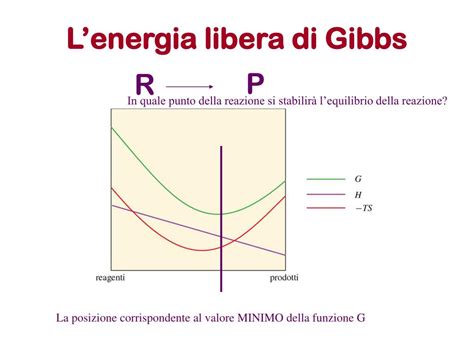
Man mano che il sistema evolve verso l'equilibrio, il valore del ΔG si avvicina a zero. All'equilibrio, ΔG = 0 e le concentrazioni di prodotti e reagenti sono quelle di equilibrio, per cui:
da cui si ricava che ΔG° = - RT ln Kc = -2,3 RT lg Kc, dove R è la costante dei gas.
Questa funzione di stato permette di determinare il lavoro utile ottenibile nella trasformazione di un sistema termodinamico a pressione e temperatura costante. La funzione equivalente in meccanica è l'energia potenziale, che rappresenta la possibilità di fare lavoro. In maniera simile, l'energia libera di Gibbs è la massima quantità di lavoro, non dovuto all'espansione meccanica, che può essere estratta da un sistema chiuso (cioè un sistema che scambia calore e lavoro con il mondo esterno, ma non scambia materia). Tale massimo lavoro può essere ottenuto solo se le trasformazioni sono reversibili.
Si consideri un sistema materiale costituito da una mole di gas ideale che passi reversibilmente da uno stato con energia libera G₁ ad uno stato finale con energia libera G₂. Se il processo è isotermo, e ΔG = G₂ - G₁. Se lo stato iniziale è quello standard, possiamo indicare come G₁° e vale 1 bar. È importante notare due fattori: l'energia libera di un gas è funzione della temperatura e della pressione, mentre l'energia libera standard dipende solo dalla temperatura. Nel caso di un gas reale, la fugacità sostituisce la pressione.
Supponiamo di voler ottenere lavoro utile tramite una pila. Il lavoro utile si differenzia dal lavoro accidentale, legato alla variazione del numero di moli gassose di prodotti e reagenti. Tale lavoro assume valore massimo in condizioni di reversibilità.
dove ΔH è l'entalpia, S l'entropia e T la temperatura. L'energia di Gibbs standard di reazione viene utilizzata per predire la direzione di una reazione chimica allo stato standard, ossia la spontaneità termodinamica della reazione.
dove ΔH è il calore scambiato dal sistema e T la temperatura a cui viene scambiato (quella del laboratorio, ad esempio). Questo risultato è notevolmente impiegato anche nello studio delle reazioni chimiche in ambiente, nella forma integrale:
, dove per i reagenti viene sommata l'opposto dell'energia libera.
Riassumendo, questa relazione indica che nelle trasformazioni a temperatura e pressione costanti l'energia libera di Gibbs diminuisce per un processo spontaneo (differenziale negativo) mentre è ad un valore minimo (differenziale nullo) per un processo reversibile, cioè in condizioni di equilibrio. Questo criterio è molto importante, in quanto di solito le trasformazioni nell'ambiente naturale ed in laboratorio avvengono a temperatura e pressione costante (piuttosto che a volume costante): è per questo che la funzione di Gibbs è più utilizzata rispetto a quella di Helmholtz.
In chimica, un fenomeno come l'osmosi è un esempio di processo spontaneo (ΔG < 0), mentre l'elettrolisi richiede il compimento di un lavoro elettrico perché implica reazioni non spontanee (ΔG > 0).
Stato Standard e Calcolo della Variazione di Energia Libera Standard
Si definisce stato standard di una sostanza lo stato di aggregazione più stabile (attività unitaria) alla pressione di stato standard, p° = 1 bar, e alla temperatura che si sta considerando. L'energia libera degli elementi nei loro stati standard assume valore uguale a zero.
Qualora non fosse noto il ΔG° di una reazione, conoscendo il ΔG° di opportune reazioni è possibile calcolare la differenza di energia libera molare standard di formazione combinando, tramite artificio matematico, queste reazioni (legge di Hess).
La somma algebrica pesata sui coefficienti stechiometrici dei potenziali chimici standard o delle energie libere standard di formazione, ΔG°f, sono per definizione la variazione di energia libera standard di reazione.
Per definizione, in condizioni di equilibrio: l'argomento del logaritmico, , noto come quoziente di reazione e che esprime lo stato del sistema nelle condizioni attuali (non standard e non di equilibrio), è in questo caso uguale alla costante d'equilibrio.
